Hybridisierung erklärt, warum Moleküle bestimmte Formen haben und warum Kohlenstoff... Prikaži več
Registriraj se za ogled vsebineBrezplačno je!
Dostop do vseh dokumentov
Izboljšaj svoje ocene
Pridruži se milijonom študentov
Knowunity AI
Predmeti
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Prikaži vse teme
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Prikaži vse teme
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Prikaži vse teme
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Prikaži vse teme
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Prikaži vse teme
1,212
•
Posodobljeno May 11, 2026
•
Hybridisierung erklärt, warum Moleküle bestimmte Formen haben und warum Kohlenstoff... Prikaži več
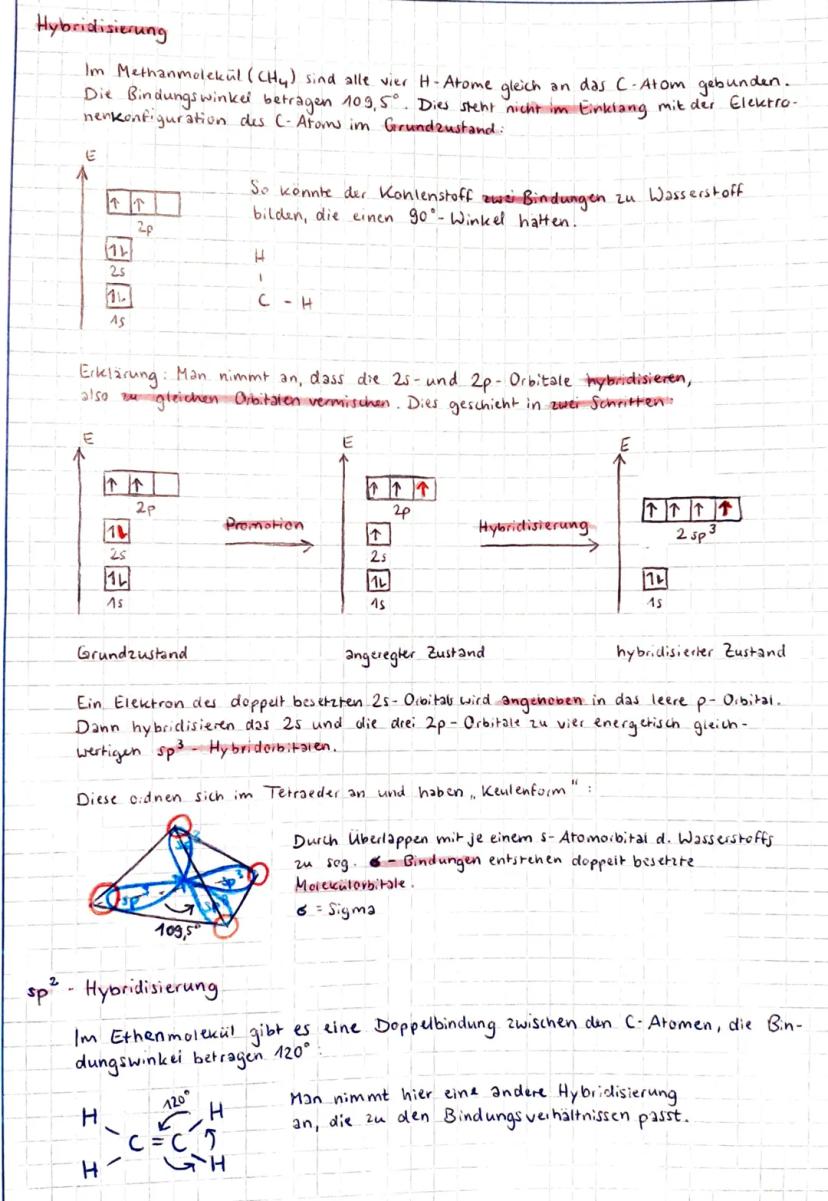
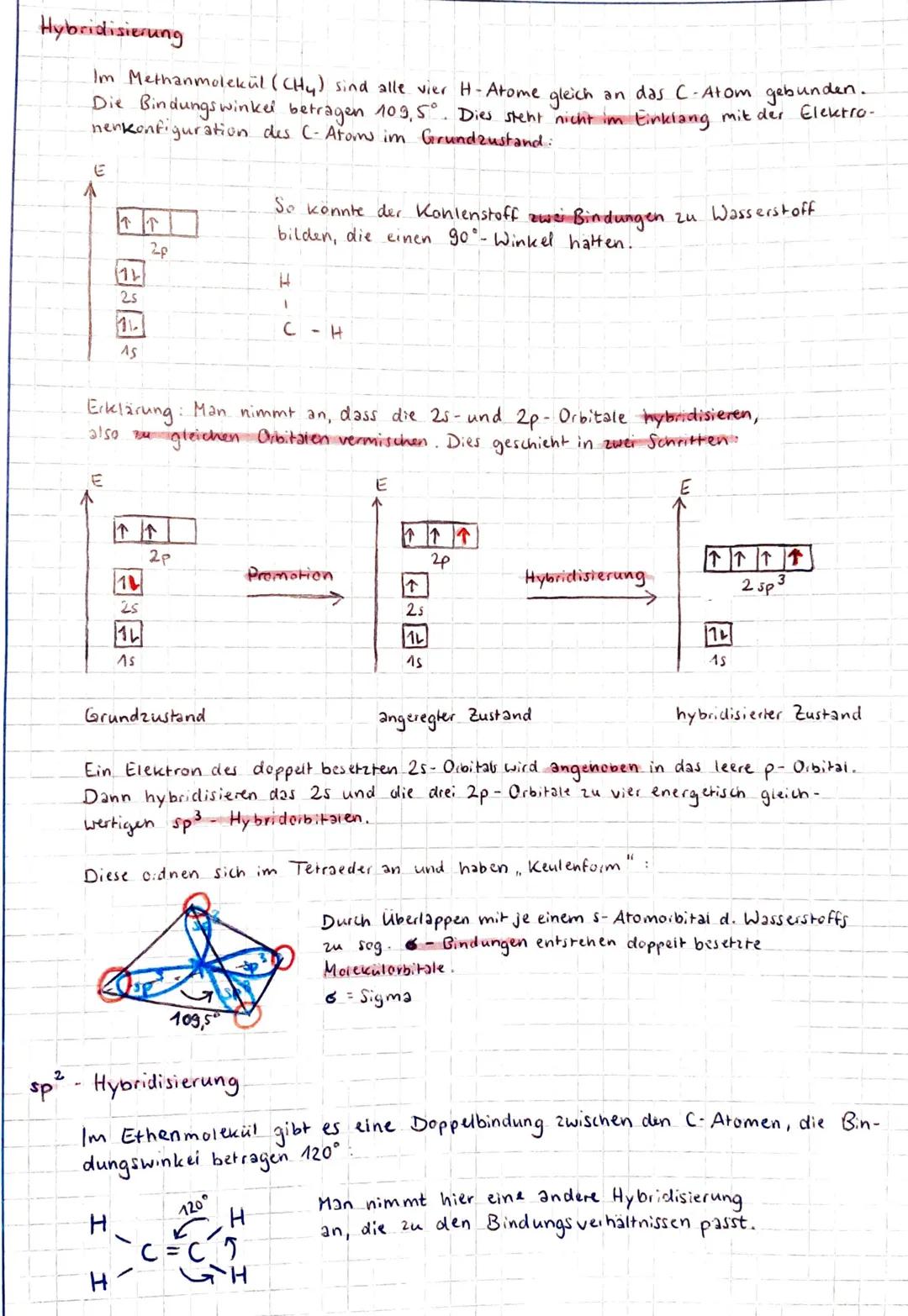
Stell dir vor, Kohlenstoff wäre ein Zauberer, der seine Orbitale neu anordnet, um perfekte Bindungen zu schaffen! Im Methanmolekül (CH₄) sind alle vier Wasserstoff-Atome identisch an das Kohlenstoff-Atom gebunden, mit einem Bindungswinkel von 109,5°.
Normalerweise hätte Kohlenstoff im Grundzustand nur zwei ungepaarte Elektronen für Bindungen. Durch Promotion wird aber ein Elektron aus dem 2s-Orbital in ein leeres 2p-Orbital angehoben.
Dann passiert die eigentliche sp³-Hybridisierung: Das 2s-Orbital und die drei 2p-Orbitale vermischen sich zu vier energetisch gleichwertigen sp³-Hybridorbitalen. Diese ordnen sich tetraedrisch an und haben eine charakteristische "Keulenform", die perfekt für σ-Bindungen mit Wasserstoff geeignet ist.
💡 Merktipp: sp³ bedeutet: 1 s-Orbital + 3 p-Orbitale = 4 hybride Orbitale = Tetraeder-Form!
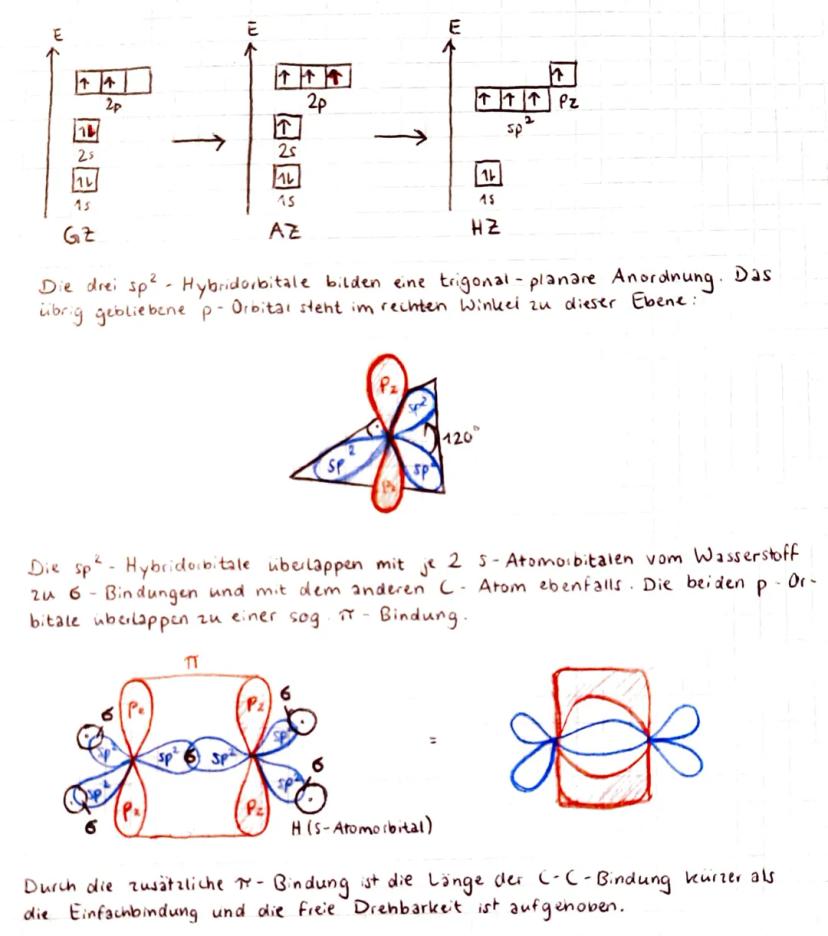
Bei Ethenmolekülen (C₂H₄) mit ihrer charakteristischen Doppelbindung läuft das Spiel etwas anders! Die Bindungswinkel betragen hier 120°, was eine völlig andere Hybridisierung erfordert.
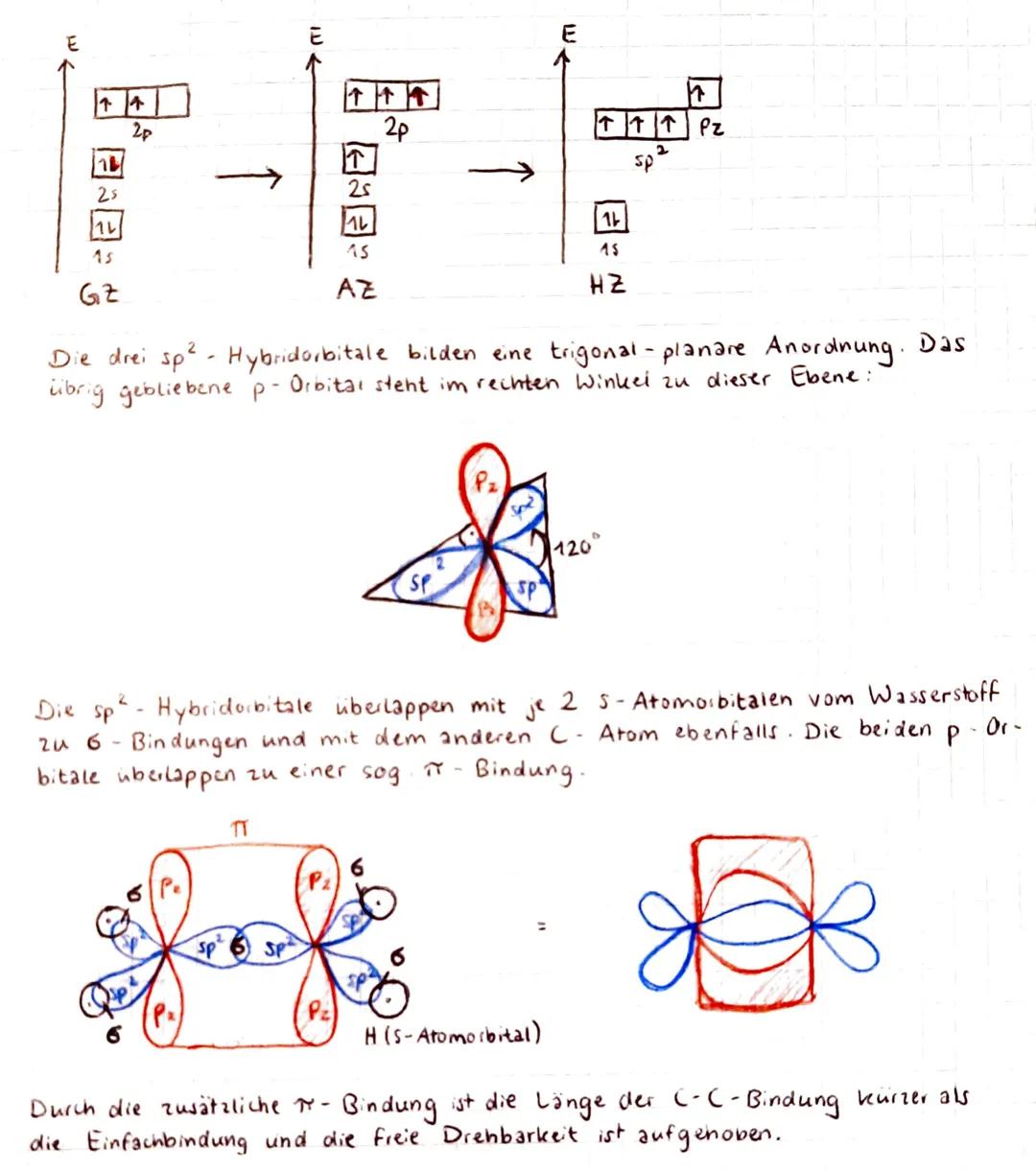
Bei der sp²-Hybridisierung vermischen sich nur das 2s-Orbital und zwei 2p-Orbitale miteinander. Das dritte p-Orbital bleibt unverändert und steht senkrecht zur Ebene der drei sp²-Hybridorbitale.
Die drei sp²-Orbitale bilden eine trigonal-planare Anordnung mit 120°-Winkeln. Während diese für σ-Bindungen sorgen, überlappen die beiden übrig gebliebenen p-Orbitale zu einer π-Bindung . Dadurch entsteht die charakteristische Doppelbindung zwischen den Kohlenstoff-Atomen.
💡 Wichtig: Durch die zusätzliche π-Bindung wird die C-C-Bindung kürzer und die freie Drehbarkeit verschwindet!
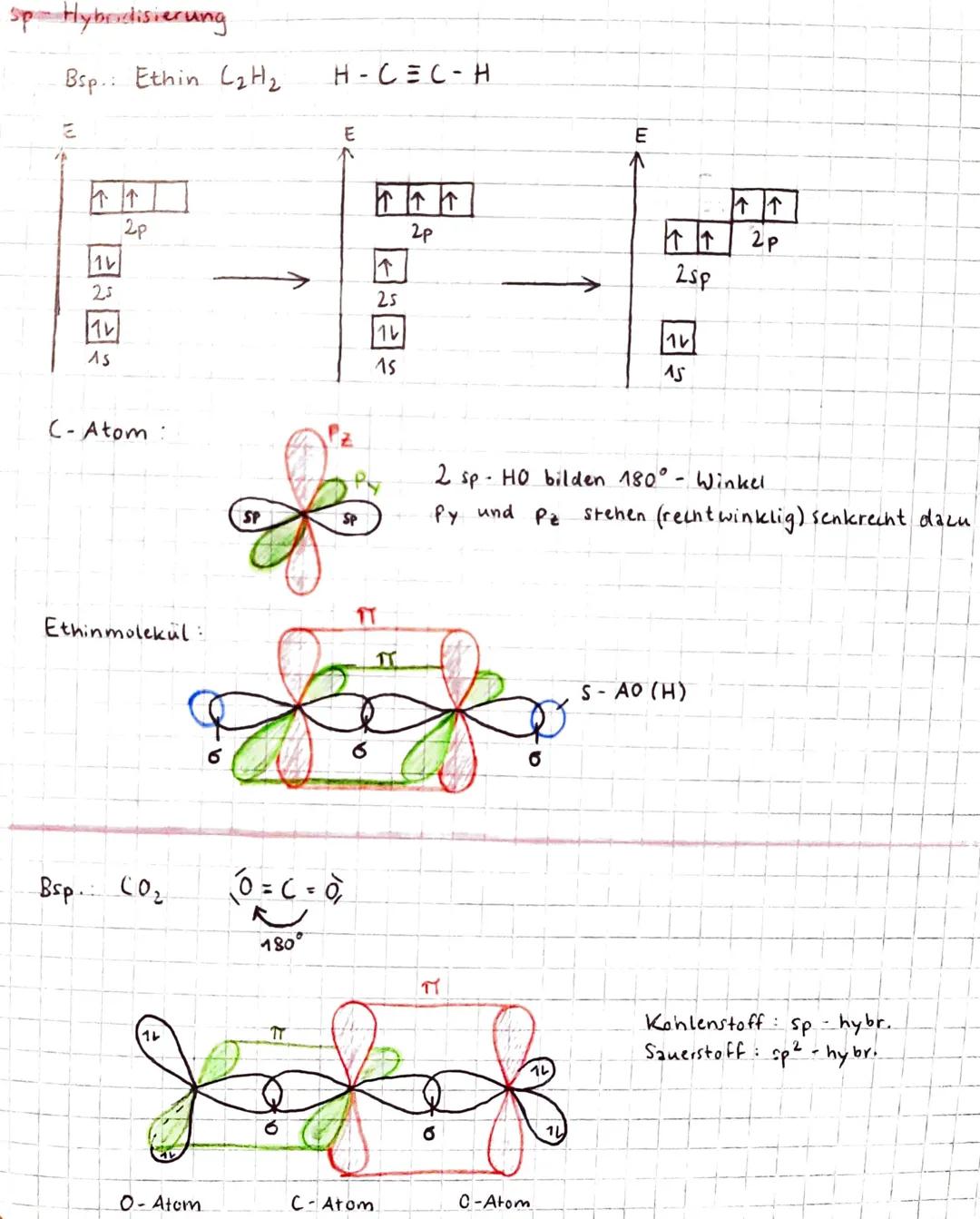
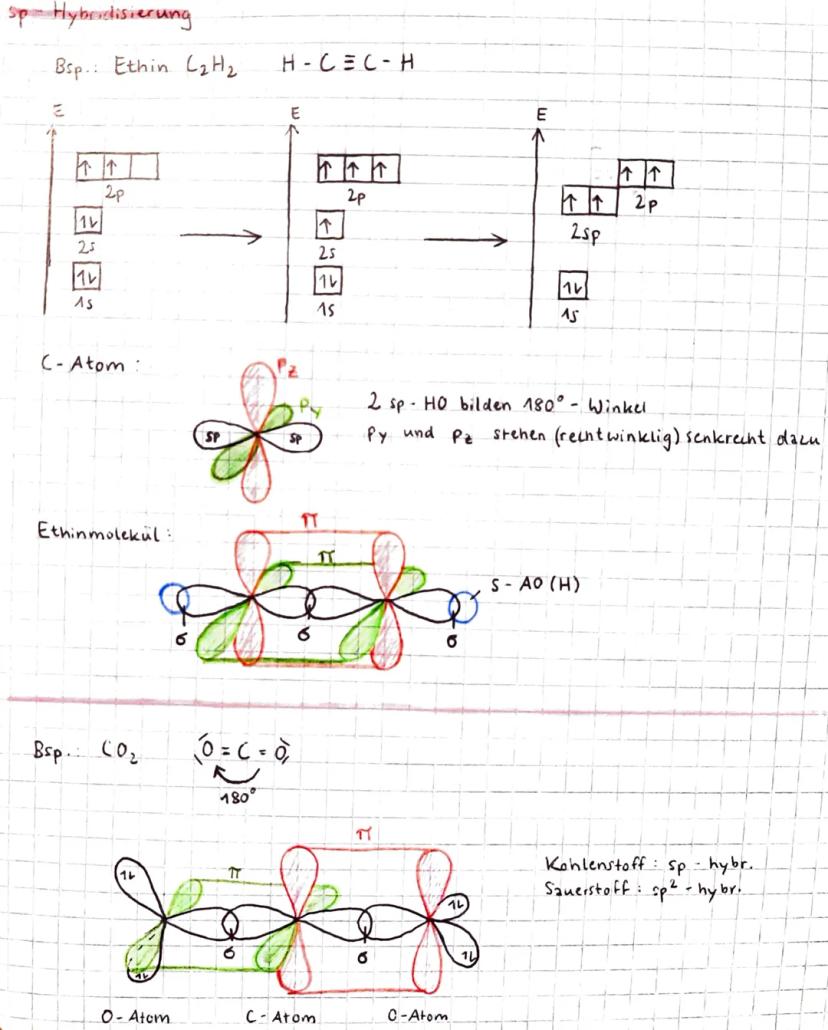
Die sp-Hybridisierung ist die minimalistischste Variante und kommt bei Dreifachbindungen wie in Ethin (C₂H₂) zum Einsatz. Hier vermischen sich nur das 2s-Orbital mit einem einzigen 2p-Orbital.
Die beiden sp-Hybridorbitale ordnen sich linear mit einem 180°-Winkel an. Die zwei übrig gebliebenen p-Orbitale (py und pz) stehen senkrecht zueinander und senkrecht zur sp-Achse.
Während die sp-Orbitale σ-Bindungen bilden, entstehen aus den beiden p-Orbitalen zwei π-Bindungen. Das Ergebnis: eine Dreifachbindung mit linearer Molekülgeometrie! Ein klassisches Beispiel ist auch CO₂, wo Kohlenstoff sp-hybridisiert ist und mit den sp²-hybridisierten Sauerstoff-Atomen lineare Moleküle bildet.
💡 Eselsbrücke: Je mehr s-Charakter (sp³ → sp² → sp), desto linearer wird das Molekül!
Naš AI Spremljevalec je orodje umetne inteligence, osredotočeno na dijake, ki ponuja več kot le odgovore. Zgrajen na milijonih virov Knowunity-ja, zagotavlja relevantne informacije, prilagojene načrte učenja, kvize in vsebino neposredno v klepetu ter se prilagaja tvoji individualni poti učenja.
Aplikacijo lahko preneseš iz Google Play Store ali Apple App Store.
Tako je! Uživaj v brezplačnem dostopu do učnih vsebin, se povezuj s sošolci in dobi takojšnjo pomoč – vse na dosegu roke.
App Store
Google Play
Aplikacija je res enostavna za uporabo in dobro oblikovana. Našel sem vse, kar sem iskal, in se iz predstavitev ogromno naučil! Aplikacijo bom zagotovo uporabil za razredno nalogo! In seveda mi je tudi super vir navdiha.
Stefan S
iOS uporabnik
Ta aplikacija je res kul. Toliko zapiskov za učenje in pomoči [...]. Moj problemski predmet je na primer francoščina, in aplikacija ima toliko možnosti za pomoč. Zahvaljujoč tej aplikaciji sem izboljšal svojo francoščino. Priporočil bi jo vsem.
Samantha Klich
Android uporabnica
Vau, res sem navdušena. Aplikacijo sem preizkusila, ker sem jo videla oglaševano večkrat, in sem bila popolnoma presenečena. Ta aplikacija je POMOČ, ki jo rabiš za šolo, in ponuja toliko stvari, kot so vaje in povzetki, ki so bili meni osebno ZELO koristni.
Anna
iOS uporabnica
Najboljša aplikacija na svetu! Ni besed, ker je preveč dobra
Thomas R
iOS uporabnik
Preprosto neverjetno. Omogoča mi učenje 10x bolje, ta aplikacija si zasluži 10/10. Toplo jo priporočam vsem. Lahko gledam in iščem zapiski. Lahko jih shranim v mapo predmeta. Kadarkoli se lahko vrnem in se učim. Če še nisi preizkusil te aplikacije, res nekaj zamujašː
Basil
Android uporabnik
Ta aplikacija me je naredila veliko bolj samozavestnega pri pripravi na izpite, ne samo zato, ker je povečala moje samozavest z funkcijami, ki ti omogočajo povezovanje z drugimi in se počutiš manj osamljen, ampak tudi zaradi načina, kako je aplikacija sama osredotočena na to, da se počutiš bolje. Enostavna je za navigacijo, zabavna za uporabo in koristna za vsakogar, ki se spopada s čimer koli.
David K
iOS uporabnik
Aplikacija je preprosto odlična! Vse kar moram naredit je, da vpišem temo v iskalno vrstico in dobim odgovor super hitro. Ne rabim gledat 10 YouTube videov, da razumem nekaj, tako da privarčujem čas. Toplo priporočam!
Sudenaz Ocak
Android uporabnica
V šoli sem bila res slaba pri matematiki, ampak zahvaljujoč aplikaciji se mi zdaj gre bolje. Tako hvaležna sem, da ste naredili to aplikacijo.
Greenlight Bonnie
uporabnica Androida
zelo zanesljiva aplikacija za pomoč in razvoj vaših idej o matematiki, angleščini in drugih sorodnih temah pri vašem delu. prosim uporabite to aplikacijo, če se spopadaš s težavami na določenih področjih, ta aplikacija je ključna za to. škoda, da nisem naredil ocene prej. in je tudi brezplačna, tako da se ne sekiriraj glede tega.
Rohan U
uporabnik Android
Vem, da veliko aplikacij uporablja lažne račune za povečanje svojih ocen, vendar si ta aplikacija zasluži vse to. Prvotno sem dobival 4 na angleških izpitih in tokrat sem dobil oceno 7. Za to aplikacijo nisem vedel do tri dni pred izpitom in mi je ZELO pomagala. Prosim, res mi zaupaj in jo uporabi, saj sem prepričan, da boš tudi ti videl napredek.
Xander S
uporabnik iOS
KVIZI IN KARTICE SO TAKO UPORABNI IN OBOŽUJEM Knowunity AI. TO JE TUDI DOBESEDNO KOT CHATGPT SAMO PAMETNEJŠI!! MI JE POMAGAL TUDI Z MOJIMI PROBLEMI Z MASKARO!! KAKOR TUDI Z MOJIMI PRAVIMI PREDMETI! SEVEDA 😍😁😲🤑💗✨🎀😮
Elisha
uporabnik iOS
Ta aplikacija je res najboljša. Se mi zdi učenje tako dolgočasno, ampak ta aplikacija naredi tako enostavno, da organiziraš vse skupaj in potem lahko vprašaš brezplačno AI, da te preizkusi, tako dobro in lahko enostavno naložiš svoje zadeve. toplo priporočam kot nekdo, ki zdaj rešuje poskusne izpite
Paul T
uporabnik iOS
Aplikacija je res enostavna za uporabo in dobro oblikovana. Našel sem vse, kar sem iskal, in se iz predstavitev ogromno naučil! Aplikacijo bom zagotovo uporabil za razredno nalogo! In seveda mi je tudi super vir navdiha.
Stefan S
iOS uporabnik
Ta aplikacija je res kul. Toliko zapiskov za učenje in pomoči [...]. Moj problemski predmet je na primer francoščina, in aplikacija ima toliko možnosti za pomoč. Zahvaljujoč tej aplikaciji sem izboljšal svojo francoščino. Priporočil bi jo vsem.
Samantha Klich
Android uporabnica
Vau, res sem navdušena. Aplikacijo sem preizkusila, ker sem jo videla oglaševano večkrat, in sem bila popolnoma presenečena. Ta aplikacija je POMOČ, ki jo rabiš za šolo, in ponuja toliko stvari, kot so vaje in povzetki, ki so bili meni osebno ZELO koristni.
Anna
iOS uporabnica
Najboljša aplikacija na svetu! Ni besed, ker je preveč dobra
Thomas R
iOS uporabnik
Preprosto neverjetno. Omogoča mi učenje 10x bolje, ta aplikacija si zasluži 10/10. Toplo jo priporočam vsem. Lahko gledam in iščem zapiski. Lahko jih shranim v mapo predmeta. Kadarkoli se lahko vrnem in se učim. Če še nisi preizkusil te aplikacije, res nekaj zamujašː
Basil
Android uporabnik
Ta aplikacija me je naredila veliko bolj samozavestnega pri pripravi na izpite, ne samo zato, ker je povečala moje samozavest z funkcijami, ki ti omogočajo povezovanje z drugimi in se počutiš manj osamljen, ampak tudi zaradi načina, kako je aplikacija sama osredotočena na to, da se počutiš bolje. Enostavna je za navigacijo, zabavna za uporabo in koristna za vsakogar, ki se spopada s čimer koli.
David K
iOS uporabnik
Aplikacija je preprosto odlična! Vse kar moram naredit je, da vpišem temo v iskalno vrstico in dobim odgovor super hitro. Ne rabim gledat 10 YouTube videov, da razumem nekaj, tako da privarčujem čas. Toplo priporočam!
Sudenaz Ocak
Android uporabnica
V šoli sem bila res slaba pri matematiki, ampak zahvaljujoč aplikaciji se mi zdaj gre bolje. Tako hvaležna sem, da ste naredili to aplikacijo.
Greenlight Bonnie
uporabnica Androida
zelo zanesljiva aplikacija za pomoč in razvoj vaših idej o matematiki, angleščini in drugih sorodnih temah pri vašem delu. prosim uporabite to aplikacijo, če se spopadaš s težavami na določenih področjih, ta aplikacija je ključna za to. škoda, da nisem naredil ocene prej. in je tudi brezplačna, tako da se ne sekiriraj glede tega.
Rohan U
uporabnik Android
Vem, da veliko aplikacij uporablja lažne račune za povečanje svojih ocen, vendar si ta aplikacija zasluži vse to. Prvotno sem dobival 4 na angleških izpitih in tokrat sem dobil oceno 7. Za to aplikacijo nisem vedel do tri dni pred izpitom in mi je ZELO pomagala. Prosim, res mi zaupaj in jo uporabi, saj sem prepričan, da boš tudi ti videl napredek.
Xander S
uporabnik iOS
KVIZI IN KARTICE SO TAKO UPORABNI IN OBOŽUJEM Knowunity AI. TO JE TUDI DOBESEDNO KOT CHATGPT SAMO PAMETNEJŠI!! MI JE POMAGAL TUDI Z MOJIMI PROBLEMI Z MASKARO!! KAKOR TUDI Z MOJIMI PRAVIMI PREDMETI! SEVEDA 😍😁😲🤑💗✨🎀😮
Elisha
uporabnik iOS
Ta aplikacija je res najboljša. Se mi zdi učenje tako dolgočasno, ampak ta aplikacija naredi tako enostavno, da organiziraš vse skupaj in potem lahko vprašaš brezplačno AI, da te preizkusi, tako dobro in lahko enostavno naložiš svoje zadeve. toplo priporočam kot nekdo, ki zdaj rešuje poskusne izpite
Paul T
uporabnik iOS
Hybridisierung erklärt, warum Moleküle bestimmte Formen haben und warum Kohlenstoff so vielseitige Bindungen eingehen kann. Anstatt in ihrer ursprünglichen Form zu bleiben, vermischen sich die Elektronen-Orbitale und schaffen neue, gleichwertige Bindungsmöglichkeiten.

Dostop do vseh dokumentov
Izboljšaj svoje ocene
Pridruži se milijonom študentov
Stell dir vor, Kohlenstoff wäre ein Zauberer, der seine Orbitale neu anordnet, um perfekte Bindungen zu schaffen! Im Methanmolekül (CH₄) sind alle vier Wasserstoff-Atome identisch an das Kohlenstoff-Atom gebunden, mit einem Bindungswinkel von 109,5°.
Normalerweise hätte Kohlenstoff im Grundzustand nur zwei ungepaarte Elektronen für Bindungen. Durch Promotion wird aber ein Elektron aus dem 2s-Orbital in ein leeres 2p-Orbital angehoben.
Dann passiert die eigentliche sp³-Hybridisierung: Das 2s-Orbital und die drei 2p-Orbitale vermischen sich zu vier energetisch gleichwertigen sp³-Hybridorbitalen. Diese ordnen sich tetraedrisch an und haben eine charakteristische "Keulenform", die perfekt für σ-Bindungen mit Wasserstoff geeignet ist.
💡 Merktipp: sp³ bedeutet: 1 s-Orbital + 3 p-Orbitale = 4 hybride Orbitale = Tetraeder-Form!

Dostop do vseh dokumentov
Izboljšaj svoje ocene
Pridruži se milijonom študentov
Bei Ethenmolekülen (C₂H₄) mit ihrer charakteristischen Doppelbindung läuft das Spiel etwas anders! Die Bindungswinkel betragen hier 120°, was eine völlig andere Hybridisierung erfordert.
Bei der sp²-Hybridisierung vermischen sich nur das 2s-Orbital und zwei 2p-Orbitale miteinander. Das dritte p-Orbital bleibt unverändert und steht senkrecht zur Ebene der drei sp²-Hybridorbitale.
Die drei sp²-Orbitale bilden eine trigonal-planare Anordnung mit 120°-Winkeln. Während diese für σ-Bindungen sorgen, überlappen die beiden übrig gebliebenen p-Orbitale zu einer π-Bindung . Dadurch entsteht die charakteristische Doppelbindung zwischen den Kohlenstoff-Atomen.
💡 Wichtig: Durch die zusätzliche π-Bindung wird die C-C-Bindung kürzer und die freie Drehbarkeit verschwindet!

Dostop do vseh dokumentov
Izboljšaj svoje ocene
Pridruži se milijonom študentov
Die sp-Hybridisierung ist die minimalistischste Variante und kommt bei Dreifachbindungen wie in Ethin (C₂H₂) zum Einsatz. Hier vermischen sich nur das 2s-Orbital mit einem einzigen 2p-Orbital.
Die beiden sp-Hybridorbitale ordnen sich linear mit einem 180°-Winkel an. Die zwei übrig gebliebenen p-Orbitale (py und pz) stehen senkrecht zueinander und senkrecht zur sp-Achse.
Während die sp-Orbitale σ-Bindungen bilden, entstehen aus den beiden p-Orbitalen zwei π-Bindungen. Das Ergebnis: eine Dreifachbindung mit linearer Molekülgeometrie! Ein klassisches Beispiel ist auch CO₂, wo Kohlenstoff sp-hybridisiert ist und mit den sp²-hybridisierten Sauerstoff-Atomen lineare Moleküle bildet.
💡 Eselsbrücke: Je mehr s-Charakter (sp³ → sp² → sp), desto linearer wird das Molekül!
Naš AI Spremljevalec je orodje umetne inteligence, osredotočeno na dijake, ki ponuja več kot le odgovore. Zgrajen na milijonih virov Knowunity-ja, zagotavlja relevantne informacije, prilagojene načrte učenja, kvize in vsebino neposredno v klepetu ter se prilagaja tvoji individualni poti učenja.
Aplikacijo lahko preneseš iz Google Play Store ali Apple App Store.
Tako je! Uživaj v brezplačnem dostopu do učnih vsebin, se povezuj s sošolci in dobi takojšnjo pomoč – vse na dosegu roke.
33
Pametna orodja NEW
Pretvori te zapiski v: ✓ 50+ vprašanj za vajo ✓ Interaktivne kartice ✓ Celoten poskusni izpit ✓ Osnove za eseje
Entdecken Sie die Löslichkeit von Alkoholen wie Ethanol in verschiedenen Lösungsmitteln und das Prinzip der Gaschromatographie. Diese Zusammenfassung behandelt die Trennung von Stoffen, die Rolle von Emulgatoren in Hautcremes und die Analyse von Gaschromatogrammen. Ideal für Studierende der Chemie, die sich auf Klausuren vorbereiten. Themen: Löslichkeit, Gaschromatographie, Emulgatoren.
Vertiefte Analyse der Säure-Base-Konzepte nach Arrhenius und Brønsted, einschließlich der Autoprotolyse von Wasser und der Neutralisationsreaktion. Erfahren Sie, wie pH-Werte berechnet werden und welche Rolle Ionen in wässrigen Lösungen spielen. Ideal für Chemie-Studierende, die sich auf Klausuren vorbereiten.
Erfahren Sie die IUPAC-Regeln zur Benennung verzweigter Alkane, einschließlich der Identifikation der längsten Kohlenstoffkette, der Nummerierung von Seitenketten und der alphabetischen Ordnung. Diese Zusammenfassung bietet klare Anleitungen zur korrekten Nomenklatur von Alkane mit Methyl- und Ethylseitenketten. Ideal für Chemie-Studierende und zur Vorbereitung auf Prüfungen.
Entdecken Sie die Grundlagen der Chemie der Kohlenhydrate, einschließlich Isomerie, Enantiomerie, Fischer- und Haworth-Projektion. Lernen Sie die Eigenschaften von Monosacchariden wie Glucose und Fructose sowie die Durchführung von Tests wie der Fehling- und Silberspiegelprobe. Diese Zusammenfassung bietet eine klare Übersicht über die chemischen Eigenschaften und Reaktionen von Zuckern und deren Bedeutung in der organischen Chemie.
Entdecke die Bedeutung von Wasserstoffbrückenbindungen für das Leben auf der Erde und ihre Rolle in Molekülen wie Wasser und DNA. Diese Zusammenfassung behandelt die Definition, Entstehung und die chemischen Eigenschaften von Wasserstoffbrücken. Ideal für Chemie-Studierende, die ein tieferes Verständnis für intermolekulare Kräfte suchen.
Dieser Lernzettel für die 11. Klasse behandelt die Grundlagen der organischen Chemie, einschließlich Stoffklassen, funktionelle Gruppen, Nomenklatur, Alkohole, chirale C-Atome, Redoxreaktionen, Carbonsäuren, intermolekulare Kräfte und das Struktur-Eigenschafts-Konzept. Ideal für Schüler, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
App Store
Google Play
Aplikacija je res enostavna za uporabo in dobro oblikovana. Našel sem vse, kar sem iskal, in se iz predstavitev ogromno naučil! Aplikacijo bom zagotovo uporabil za razredno nalogo! In seveda mi je tudi super vir navdiha.
Stefan S
iOS uporabnik
Ta aplikacija je res kul. Toliko zapiskov za učenje in pomoči [...]. Moj problemski predmet je na primer francoščina, in aplikacija ima toliko možnosti za pomoč. Zahvaljujoč tej aplikaciji sem izboljšal svojo francoščino. Priporočil bi jo vsem.
Samantha Klich
Android uporabnica
Vau, res sem navdušena. Aplikacijo sem preizkusila, ker sem jo videla oglaševano večkrat, in sem bila popolnoma presenečena. Ta aplikacija je POMOČ, ki jo rabiš za šolo, in ponuja toliko stvari, kot so vaje in povzetki, ki so bili meni osebno ZELO koristni.
Anna
iOS uporabnica
Najboljša aplikacija na svetu! Ni besed, ker je preveč dobra
Thomas R
iOS uporabnik
Preprosto neverjetno. Omogoča mi učenje 10x bolje, ta aplikacija si zasluži 10/10. Toplo jo priporočam vsem. Lahko gledam in iščem zapiski. Lahko jih shranim v mapo predmeta. Kadarkoli se lahko vrnem in se učim. Če še nisi preizkusil te aplikacije, res nekaj zamujašː
Basil
Android uporabnik
Ta aplikacija me je naredila veliko bolj samozavestnega pri pripravi na izpite, ne samo zato, ker je povečala moje samozavest z funkcijami, ki ti omogočajo povezovanje z drugimi in se počutiš manj osamljen, ampak tudi zaradi načina, kako je aplikacija sama osredotočena na to, da se počutiš bolje. Enostavna je za navigacijo, zabavna za uporabo in koristna za vsakogar, ki se spopada s čimer koli.
David K
iOS uporabnik
Aplikacija je preprosto odlična! Vse kar moram naredit je, da vpišem temo v iskalno vrstico in dobim odgovor super hitro. Ne rabim gledat 10 YouTube videov, da razumem nekaj, tako da privarčujem čas. Toplo priporočam!
Sudenaz Ocak
Android uporabnica
V šoli sem bila res slaba pri matematiki, ampak zahvaljujoč aplikaciji se mi zdaj gre bolje. Tako hvaležna sem, da ste naredili to aplikacijo.
Greenlight Bonnie
uporabnica Androida
zelo zanesljiva aplikacija za pomoč in razvoj vaših idej o matematiki, angleščini in drugih sorodnih temah pri vašem delu. prosim uporabite to aplikacijo, če se spopadaš s težavami na določenih področjih, ta aplikacija je ključna za to. škoda, da nisem naredil ocene prej. in je tudi brezplačna, tako da se ne sekiriraj glede tega.
Rohan U
uporabnik Android
Vem, da veliko aplikacij uporablja lažne račune za povečanje svojih ocen, vendar si ta aplikacija zasluži vse to. Prvotno sem dobival 4 na angleških izpitih in tokrat sem dobil oceno 7. Za to aplikacijo nisem vedel do tri dni pred izpitom in mi je ZELO pomagala. Prosim, res mi zaupaj in jo uporabi, saj sem prepričan, da boš tudi ti videl napredek.
Xander S
uporabnik iOS
KVIZI IN KARTICE SO TAKO UPORABNI IN OBOŽUJEM Knowunity AI. TO JE TUDI DOBESEDNO KOT CHATGPT SAMO PAMETNEJŠI!! MI JE POMAGAL TUDI Z MOJIMI PROBLEMI Z MASKARO!! KAKOR TUDI Z MOJIMI PRAVIMI PREDMETI! SEVEDA 😍😁😲🤑💗✨🎀😮
Elisha
uporabnik iOS
Ta aplikacija je res najboljša. Se mi zdi učenje tako dolgočasno, ampak ta aplikacija naredi tako enostavno, da organiziraš vse skupaj in potem lahko vprašaš brezplačno AI, da te preizkusi, tako dobro in lahko enostavno naložiš svoje zadeve. toplo priporočam kot nekdo, ki zdaj rešuje poskusne izpite
Paul T
uporabnik iOS
Aplikacija je res enostavna za uporabo in dobro oblikovana. Našel sem vse, kar sem iskal, in se iz predstavitev ogromno naučil! Aplikacijo bom zagotovo uporabil za razredno nalogo! In seveda mi je tudi super vir navdiha.
Stefan S
iOS uporabnik
Ta aplikacija je res kul. Toliko zapiskov za učenje in pomoči [...]. Moj problemski predmet je na primer francoščina, in aplikacija ima toliko možnosti za pomoč. Zahvaljujoč tej aplikaciji sem izboljšal svojo francoščino. Priporočil bi jo vsem.
Samantha Klich
Android uporabnica
Vau, res sem navdušena. Aplikacijo sem preizkusila, ker sem jo videla oglaševano večkrat, in sem bila popolnoma presenečena. Ta aplikacija je POMOČ, ki jo rabiš za šolo, in ponuja toliko stvari, kot so vaje in povzetki, ki so bili meni osebno ZELO koristni.
Anna
iOS uporabnica
Najboljša aplikacija na svetu! Ni besed, ker je preveč dobra
Thomas R
iOS uporabnik
Preprosto neverjetno. Omogoča mi učenje 10x bolje, ta aplikacija si zasluži 10/10. Toplo jo priporočam vsem. Lahko gledam in iščem zapiski. Lahko jih shranim v mapo predmeta. Kadarkoli se lahko vrnem in se učim. Če še nisi preizkusil te aplikacije, res nekaj zamujašː
Basil
Android uporabnik
Ta aplikacija me je naredila veliko bolj samozavestnega pri pripravi na izpite, ne samo zato, ker je povečala moje samozavest z funkcijami, ki ti omogočajo povezovanje z drugimi in se počutiš manj osamljen, ampak tudi zaradi načina, kako je aplikacija sama osredotočena na to, da se počutiš bolje. Enostavna je za navigacijo, zabavna za uporabo in koristna za vsakogar, ki se spopada s čimer koli.
David K
iOS uporabnik
Aplikacija je preprosto odlična! Vse kar moram naredit je, da vpišem temo v iskalno vrstico in dobim odgovor super hitro. Ne rabim gledat 10 YouTube videov, da razumem nekaj, tako da privarčujem čas. Toplo priporočam!
Sudenaz Ocak
Android uporabnica
V šoli sem bila res slaba pri matematiki, ampak zahvaljujoč aplikaciji se mi zdaj gre bolje. Tako hvaležna sem, da ste naredili to aplikacijo.
Greenlight Bonnie
uporabnica Androida
zelo zanesljiva aplikacija za pomoč in razvoj vaših idej o matematiki, angleščini in drugih sorodnih temah pri vašem delu. prosim uporabite to aplikacijo, če se spopadaš s težavami na določenih področjih, ta aplikacija je ključna za to. škoda, da nisem naredil ocene prej. in je tudi brezplačna, tako da se ne sekiriraj glede tega.
Rohan U
uporabnik Android
Vem, da veliko aplikacij uporablja lažne račune za povečanje svojih ocen, vendar si ta aplikacija zasluži vse to. Prvotno sem dobival 4 na angleških izpitih in tokrat sem dobil oceno 7. Za to aplikacijo nisem vedel do tri dni pred izpitom in mi je ZELO pomagala. Prosim, res mi zaupaj in jo uporabi, saj sem prepričan, da boš tudi ti videl napredek.
Xander S
uporabnik iOS
KVIZI IN KARTICE SO TAKO UPORABNI IN OBOŽUJEM Knowunity AI. TO JE TUDI DOBESEDNO KOT CHATGPT SAMO PAMETNEJŠI!! MI JE POMAGAL TUDI Z MOJIMI PROBLEMI Z MASKARO!! KAKOR TUDI Z MOJIMI PRAVIMI PREDMETI! SEVEDA 😍😁😲🤑💗✨🎀😮
Elisha
uporabnik iOS
Ta aplikacija je res najboljša. Se mi zdi učenje tako dolgočasno, ampak ta aplikacija naredi tako enostavno, da organiziraš vse skupaj in potem lahko vprašaš brezplačno AI, da te preizkusi, tako dobro in lahko enostavno naložiš svoje zadeve. toplo priporočam kot nekdo, ki zdaj rešuje poskusne izpite
Paul T
uporabnik iOS